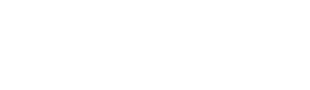上海师范大学赵宝国教授团队以带有方酸侧链的双功能手性吡哆醛为催化剂,运用羰基催化的策略,实现了苄胺α C–H键对醛的直接不对称加成反应,该工作是合成重要化合物手性β-氨基醇的最直接高效的方法之一。研究成果以题为“Catalytic asymmetric α C(sp3)–H addition of benzylamines to aldehydes”发表在最新一期《Nature Catalysis》期刊(IF=40.7)上。

论文第一作者:侯承康
手性胺是一类非常重要的化合物,在医药、天然产物、精细化学品、材料、催化等领域都有广泛应用,发展手性胺的高效构建新策略有重要意义。简单伯胺,如苄胺,是一类易得的化工原料,其α C-H键的直接官能团化是合成手性胺的高效新策略。但该反应面临两个巨大挑战:伯胺的NH2基团反应活性高,严重干扰转化;苄胺的α C-H键酸度极低(pKa ~ 42.7),难以活化。本研究工作以仿生的手性吡哆醛为催化剂,运用羰基催化的策略,突破苄胺α C-H键的反应惰性,无需对NH2基团进行保护,在温和条件下实现苄胺α C-H键对醛的不对称加成,高效构建重要化合物手性β-氨基醇。

苄胺的 α C-H 官能化
羰基催化能促进伯胺α C-H键的直接不对称转化,是一种受生物过程启发的新型催化模式,已被成功地应用于甘氨酸酯的不对称仿生Mannich反应、仿生Aldol反应、α-C Michael加成反应和α-C烯丙基化等反应。然而,到目前为止,该策略主要局限于含有强吸电子基团的活化伯胺,例如α-氨基酸酯(pKa~24)、(2-吡啶基)甲胺等。为了实现惰性伯胺化合物苄胺的α C-H键的转化,作者发展了一系列含有方酸侧链的手性吡哆醛催化剂,并应用于苄胺α C-H键对芳基醛的不对称加成反应。在筛选出最佳的催化剂以及反应条件后,对反应的底物进行了考察,各种芳基甲胺和芳基醛都能很好地适用于该转化,以较好的收率和优秀的非对映选择性、对映选择性得到一系列的手性β-氨基醇化合物。

底物的拓展
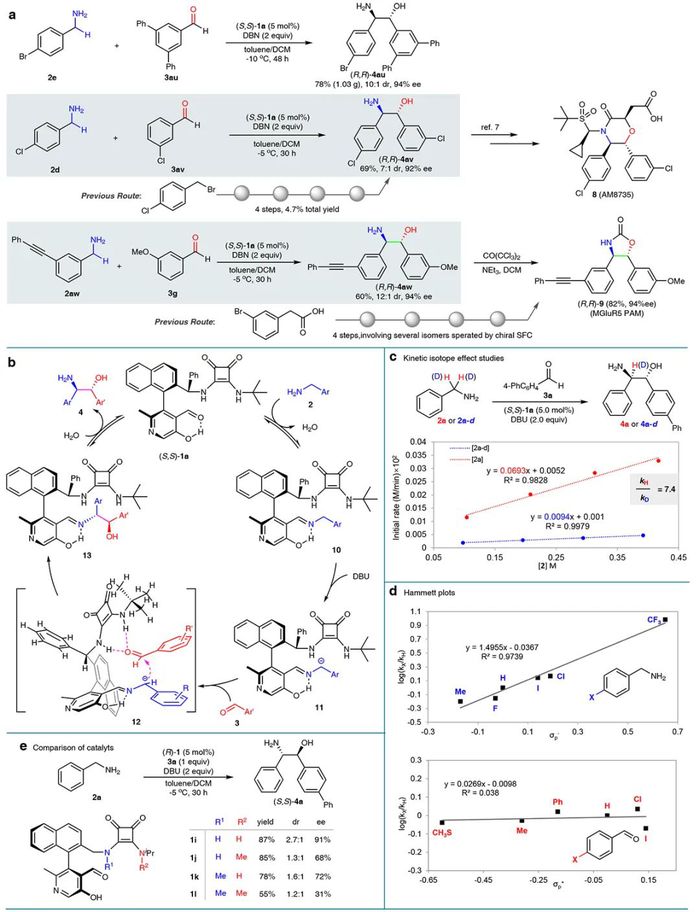
机理研究
机理研究表明该反应经历了羰基催化的反应历程,其中苄胺α C-H键的去质子化是反应的决速步,方酸侧链上的苯基以及叔丁基对于反应的立体选择性控制起着重要作用。苄胺α C-H键的活化是通过与吡哆醛催化剂形成亚胺实现的,计算化学研究表明该 C-H键的pKa值由42.7提高到24.4,酸性提高了10的18次方倍,展示了仿生吡哆醛催化剂的强大活化能力。该研究工作不仅提供了重要化合物β-氨基醇的高效构建新方法,进一步发展了羰基催化化学,还拓展了维生素B6核心骨架在仿生不对称催化中的应用。

赵宝国教授研究团队
该工作得到了教育部、国家自然科学基金委、上海市教科委、上海师范大学、上海市仿生催化前沿科学研究基地等的资金支持。